eCTD247
雲端 SaaS 電子送件平台 — eCTD 4.0 先驅,全球 450+ 生命科學客戶信賴使用
eCTD247 是 Ennov 的雲端 SaaS 平台,用於建構、管理、驗證和追蹤 eCTD(電子通用技術文件)法規送件。以「簡單、快速且經濟實惠」為定位,eCTD247 使製藥和生技公司無需傳統企業級出版系統的複雜性和成本即可組裝和提交法規檔案。
Ennov 是 eCTD 4.0 的先驅 — 全球僅四家技術供應商之一成功向 EMA 提交 eCTD 4.0 測試序列,在 EMA、FDA 和 PMDA 完成 11 次成功的 eCTD 4.0 試點送件。公司服務 450+ 家生命科學客戶,全球擁有 500,000+ 使用者。

全球 eCTD 法規更新 — 涵蓋 eCTD 版本升級、區域規範差異及實施時程等關鍵變化
Ennov 法規出版產品組合
eCTD247 定位為 Ennov 三層法規出版產品組合中的入門級方案:
| 產品 | 類型 | 目標客群 |
|---|---|---|
| eCTD247 | 雲端 SaaS | 中小型藥廠、生技新創、送件量較低的公司 |
| Ennov Dossier | 企業級出版(Ennov 原生) | 需要完整檔案生命週期管理的中大型藥廠 |
| Ennov InSight Publishing | 企業級出版(收購自 Calyx/Liquent) | 大型/前五大藥廠、複雜的全球送件 |
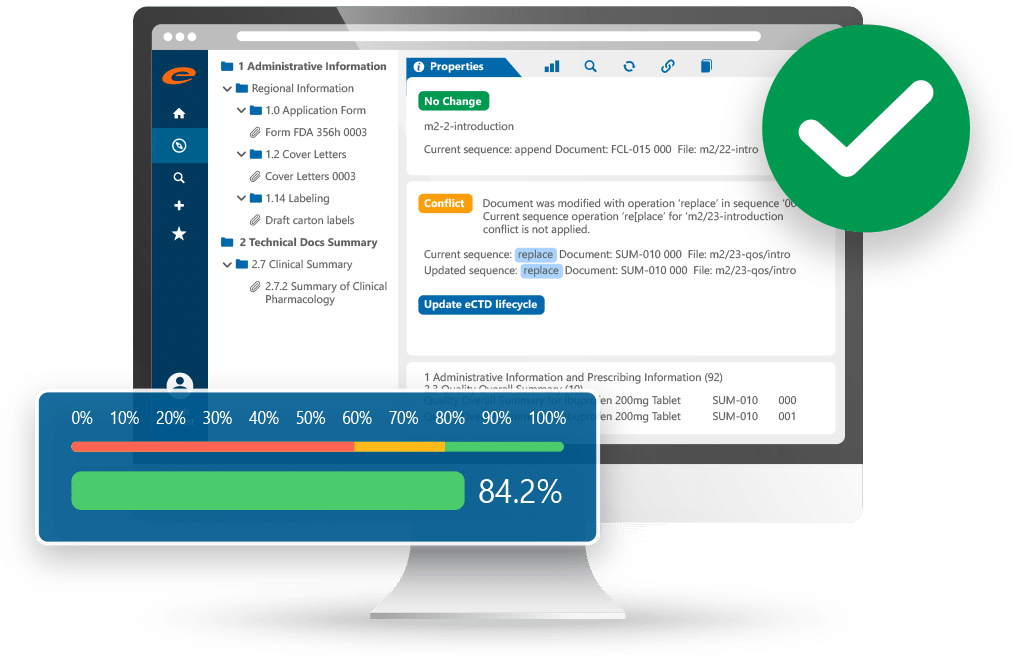
eCTD247 送件管理 — eCTD 文件樹狀結構、生命週期管理與驗證進度追蹤
核心功能
eCTD 送件建構與出版
建構、出版、驗證和提交 IND、NDA、ANDA、BLA、MAA 申請。支援 eCTD、NeeS、VNeeS、CTD(紙本)、eCopy 等格式,含 STF 生成與自動計算參考文獻
文件管理(整合 EDMS)
基於元數據的架構實現快速文件檢索,可配置的資料庫檢視和搜尋引擎,文件驗證工作流程、簽入/簽出協調機制與完整版本管理
驗證與品質保證
內建 EMA 核准的 eCTD 驗證引擎,提供全面的互動式報告。支援進階超連結分析、書籤驗證、STF 驗證,以及 IQ/OQ/PQ 驗證服務
協作與安全性
網頁式介面隨時隨地存取,雙重驗證和 SSL 加密,公開/私人工作群組存取控制,同步審閱和電子簽章,完全符合 21 CFR Part 11
雲端優勢(Premium 方案)
自動軟體更新即時反映法規標準變更,宣稱降低 48% 成本,無需 IT 資源維護,資料託管於美國或歐盟,包含 30 天免費試用
eCTD 4.0 準備度
全球僅四家供應商之一成功向 EMA 提交 eCTD 4.0 測試序列,完成 11 次試點送件(8 個 EMA + 3 個 FDA),與頂級藥廠合作進行 PMDA eCTD 4.0 試點
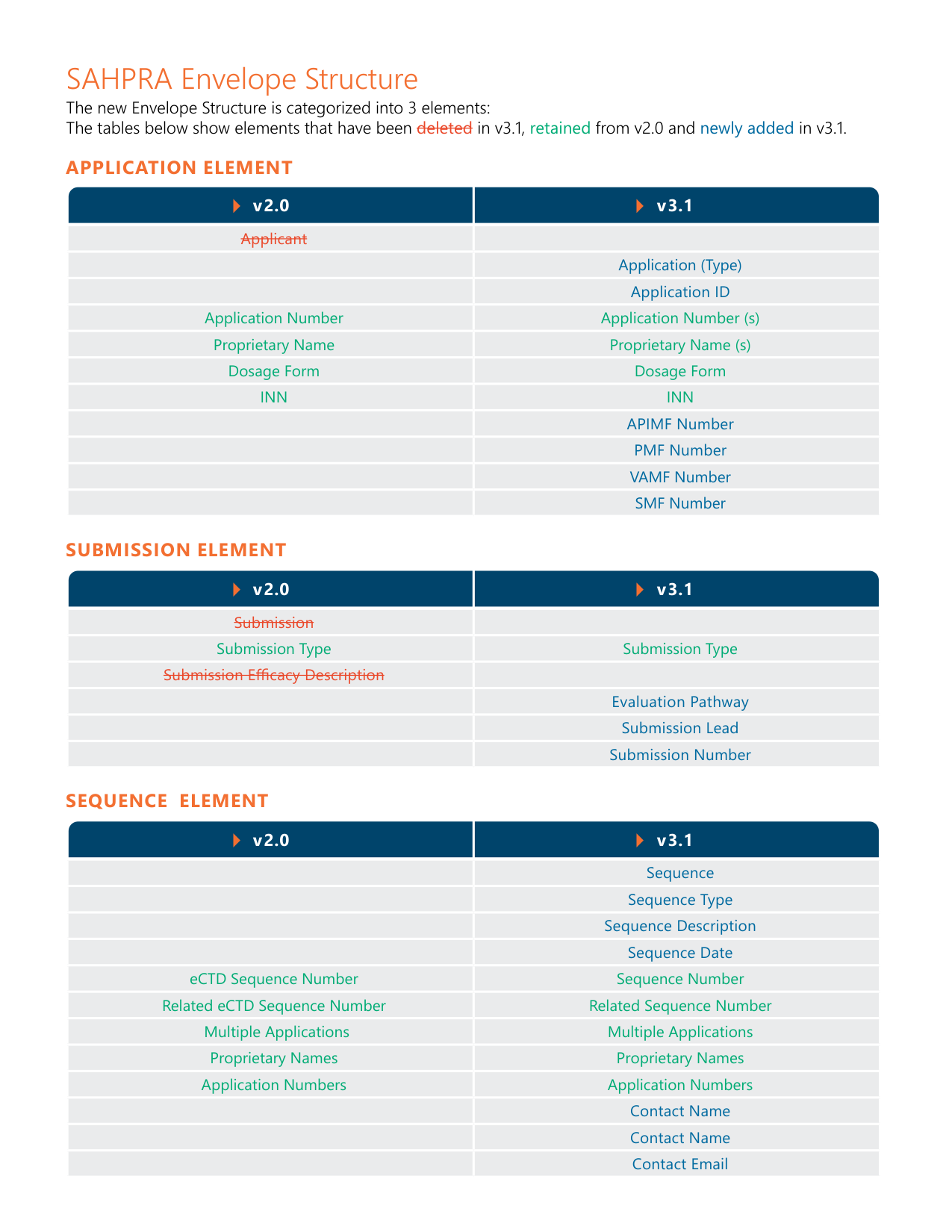
SAHPRA eCTD v2.0 與 v3.1 結構對照 — 色彩標記顯示新增、保留與刪除的元素變化
技術規格
| 規格 | 詳情 |
|---|---|
| 架構(Premium) | 100% 雲端 SaaS |
| 架構(Enterprise) | 客戶基礎設施上的本地部署 |
| 資料託管 | 美國或歐盟資料中心(客戶選擇) |
| eCTD 版本 | eCTD v3.x(現行)、eCTD v4.0(透過 InSight Publishing) |
| 支援格式 | eCTD、CTD(紙本)、NeeS、VNeeS、eCopy(含 510(k)、PMA) |
| 送件類型 | IND、NDA、ANDA、BLA、MAA |
| 驗證器 | 內建 EMA 核准的 eCTD 驗證引擎 |
| 合規性 | 21 CFR Part 11、ISO 9001:2008 |
| 安全性 | 雙重驗證、SSL 加密、存取控制 |
| EDMS | 整合 Ennov Doc EDM(Premium 方案) |
| DIA 參考模型 | 預先配置符合 DIA EDM 參考模型 |
支援區域與 eCTD 4.0 時程
| 區域 / 主管機關 | 現行狀態 | eCTD 4.0 時程 |
|---|---|---|
| FDA(美國) | NDA/BLA/ANDA/IND 強制 eCTD | v4.0 自 2024 年 9 月自願;~2029 年強制 |
| EMA(歐盟) | 所有集中程序強制 eCTD | v4.0 自 2025 年 12 月可選;2028 年強制 |
| PMDA(日本) | eCTD 接受中 | v4.0 自 2026 年 4 月強制 |
| Health Canada(加拿大) | NDS/SNDS/ANDS 強制 eCTD | v4.0 2026 年可選;2028 年強制 |
| TGA(澳洲) | 處方藥要求 eCTD | v4.0 技術試點 H1 2025 |
| SAHPRA(南非) | 自 2024 年 10 月起透過入口網站強制 | 模組 1 v3.1 自 2024 年 11 月生效 |
| Swissmedic(瑞士) | eCTD 接受中 | 2026 年試點;2028 年強制 |
| GCC | eCTD 接受中 | 適用區域模組 1 規範 |
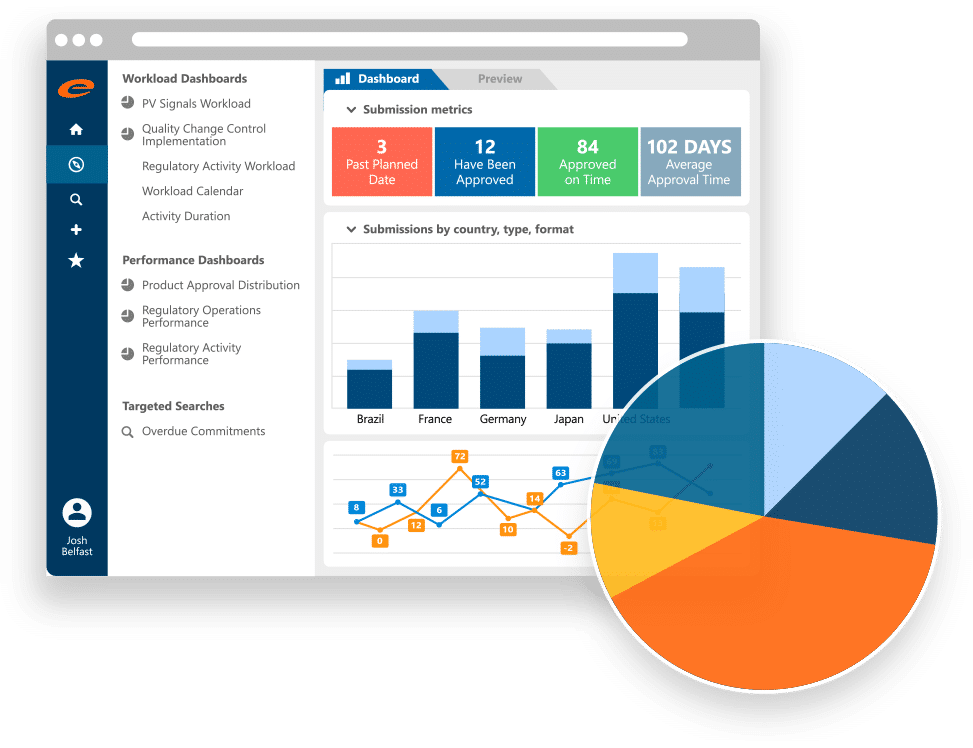
Ennov RIM — 全球法規資訊管理儀表板,涵蓋送件指標、國家分布與審核時程分析
應用領域
製藥
eCTD 送件建構、檔案生命週期管理、法規出版、NDA/ANDA/BLA/MAA 申請。
生物科技
IND/BLA 送件、法規檔案組裝、多區域送件管理。
學名藥
ANDA 送件、經濟實惠的 eCTD 出版方案。
委託研究機構(CRO)
為委託者提供出版服務、多客戶送件管理。
動物保健
獸醫 NeeS(VNeeS)送件、法規合規。
醫療器材
eCopy 送件(510(k)、PMA)。
競爭比較
| 功能 | Ennov | Lorenz docuBridge | Certara GlobalSubmit | Veeva Vault Submissions |
|---|---|---|---|---|
| 部署方式 | 雲端、本地、混合 | 本地或託管 | 僅雲端 SaaS | 僅雲端 SaaS |
| eCTD 4.0 | 11 次試點(EMA/FDA/PMDA) | 前向相容 | 已就緒 | 已就緒 |
| 整合 EDMS | 原生(Ennov Doc) | 外部 | 無 | 原生(Vault) |
| 驗證器 | 內建(EMA 核准) | 捆綁(eValidator) | 內建 | 內建 |
| AI 功能 | 是(原生,v11.0) | 有限 | 有限 | 中等 |
| 送件傳承 | 100 萬+(Calyx/InSight) | 未揭露 | 150 萬+ | 未揭露 |
關鍵差異化因素
三層產品組合
唯一提供自助式 SaaS(eCTD247)、企業原生(Dossier)和企業收購方案(InSight Publishing)的供應商 — 從新創到前五大藥廠全覆蓋
eCTD 4.0 領先地位
僅 4 家完成 EMA 試點的供應商之一;11 次試點送件為業界最高之列
快速創造價值
eCTD247 Premium「數天內」即可上線運作,含 30 天免費試用。雲端模式宣稱可降低 48% 成本
100 萬+ 送件傳承
Calyx/InSight Publishing 超過 100 萬次全球法規送件的紀錄,部署靈活性支援雲端或本地隨時切換

eCTD247 電子簽章 — 符合 21 CFR Part 11 的文件簽署、分發與生命週期管理
客戶與產業驗證
| 指標 | 數據 |
|---|---|
| 生命科學客戶 | 450+ 家 |
| 全球使用者 | 500,000+ |
| 全球法規送件 | 100 萬+ 次(透過 Calyx/InSight 傳承) |
| 專案準時交付率 | 98.5% |
| 維護續約率 | 96% |
| 客戶稽核成功率 | 100% |
相關產品推薦
了解 eCTD247
加速您的藥品上市申請流程,確保全球法規合規,立即體驗 30 天免費試用
聯絡我們了解更多