eCTD247
云端 SaaS 电子送件平台 — eCTD 4.0 先驱,全球 450+ 生命科学客户信赖使用
eCTD247 是 Ennov 的云端 SaaS 平台,用于建构、管理、验证和追踪 eCTD(电子通用技术文档)法规送件。以「简单、快速且经济实惠」为定位,eCTD247 使制药和生技公司无需传统企业级出版系统的复杂性和成本即可组装和提交法规文件。
Ennov 是 eCTD 4.0 的先驱 — 全球仅四家技术供应商之一成功向 EMA 提交 eCTD 4.0 测试串行,在 EMA、FDA 和 PMDA 完成 11 次成功的 eCTD 4.0 试点送件。公司服务 450+ 家生命科学客户,全球拥有 500,000+ 用户。

全球 eCTD 法规更新 — 涵盖 eCTD 版本升级、区域规范差异及实施时程等关键变化
Ennov 法规出版产品组合
eCTD247 定位为 Ennov 三层法规出版产品组合中的入门级方案:
| 产品 | 类型 | 目标客群 |
|---|---|---|
| eCTD247 | 云端 SaaS | 中小型药厂、生技新创、送件量较低的公司 |
| Ennov Dossier | 企业级出版(Ennov 原生) | 需要完整文件生命周期管理的中大型药厂 |
| Ennov InSight Publishing | 企业级出版(收购自 Calyx/Liquent) | 大型/前五大药厂、复杂的全球送件 |
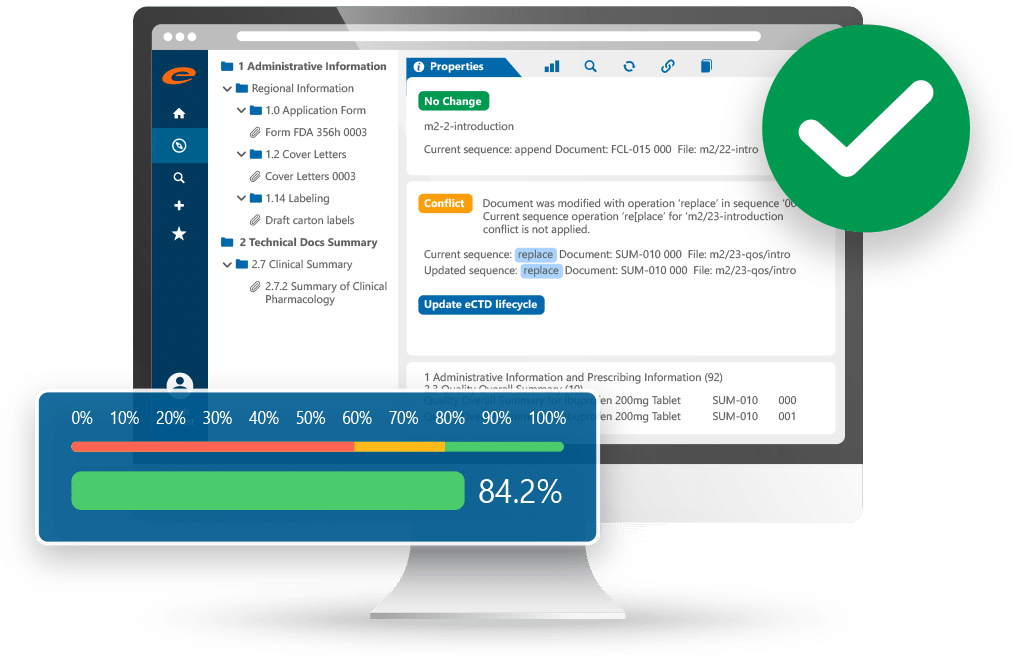
eCTD247 送件管理 — eCTD 文档树状结构、生命周期管理与验证进度追踪
内核功能
eCTD 送件建构与出版
建构、出版、验证和提交 IND、NDA、ANDA、BLA、MAA 申请。支持 eCTD、NeeS、VNeeS、CTD(纸本)、eCopy 等格式,含 STF 生成与自动计算参考文献
文档管理(集成 EDMS)
基于元数据的架构实现快速文档检索,可配置的数据库查看和搜索引擎,文档验证工作流程、签入/签出协调机制与完整版本管理
验证与品质保证
内置 EMA 核准的 eCTD 验证引擎,提供全面的交互式报告。支持高端超链接分析、书签验证、STF 验证,以及 IQ/OQ/PQ 验证服务
协作与安全性
网页式接口随时随地访问,双重验证和 SSL 加密,公开/私人工作群组访问控制,同步审阅和电子签章,完全符合 21 CFR Part 11
云端优势(Premium 方案)
自动软件更新即时反映法规标准变更,宣称降低 48% 成本,无需 IT 资源维护,数据托管于美国或欧盟,包含 30 天免费试用
eCTD 4.0 准备度
全球仅四家供应商之一成功向 EMA 提交 eCTD 4.0 测试串行,完成 11 次试点送件(8 个 EMA + 3 个 FDA),与顶级药厂合作进行 PMDA eCTD 4.0 试点
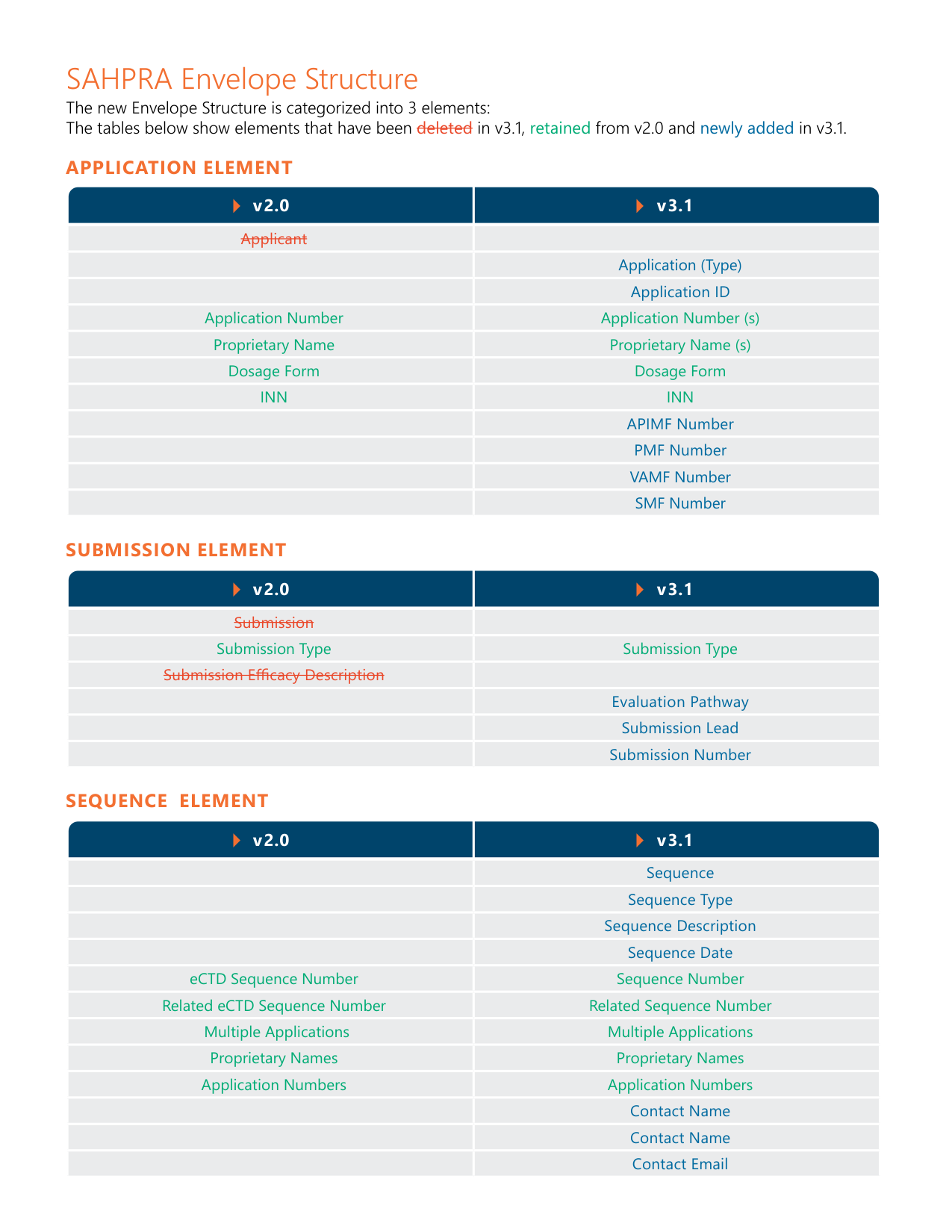
SAHPRA eCTD v2.0 与 v3.1 结构对照 — 色彩标记显示添加、保留与删除的元素变化
技术规格
| 规格 | 详情 |
|---|---|
| 架构(Premium) | 100% 云端 SaaS |
| 架构(Enterprise) | 客户基础设施上的本地部署 |
| 数据托管 | 美国或欧盟数据中心(客户选择) |
| eCTD 版本 | eCTD v3.x(现行)、eCTD v4.0(通过 InSight Publishing) |
| 支持格式 | eCTD、CTD(纸本)、NeeS、VNeeS、eCopy(含 510(k)、PMA) |
| 送件类型 | IND、NDA、ANDA、BLA、MAA |
| 验证器 | 内置 EMA 核准的 eCTD 验证引擎 |
| 合规性 | 21 CFR Part 11、ISO 9001:2008 |
| 安全性 | 双重验证、SSL 加密、访问控制 |
| EDMS | 集成 Ennov Doc EDM(Premium 方案) |
| DIA 参考模型 | 预先配置符合 DIA EDM 参考模型 |
支持区域与 eCTD 4.0 时程
| 区域 / 主管机关 | 现行状态 | eCTD 4.0 时程 |
|---|---|---|
| FDA(美国) | NDA/BLA/ANDA/IND 强制 eCTD | v4.0 自 2024 年 9 月自愿;~2029 年强制 |
| EMA(欧盟) | 所有集中进程强制 eCTD | v4.0 自 2025 年 12 月可选;2028 年强制 |
| PMDA(日本) | eCTD 接受中 | v4.0 自 2026 年 4 月强制 |
| Health Canada(加拿大) | NDS/SNDS/ANDS 强制 eCTD | v4.0 2026 年可选;2028 年强制 |
| TGA(澳洲) | 处方药要求 eCTD | v4.0 技术试点 H1 2025 |
| SAHPRA(南非) | 自 2024 年 10 月起通过门户网站强制 | 模块 1 v3.1 自 2024 年 11 月生效 |
| Swissmedic(瑞士) | eCTD 接受中 | 2026 年试点;2028 年强制 |
| GCC | eCTD 接受中 | 适用区域模块 1 规范 |
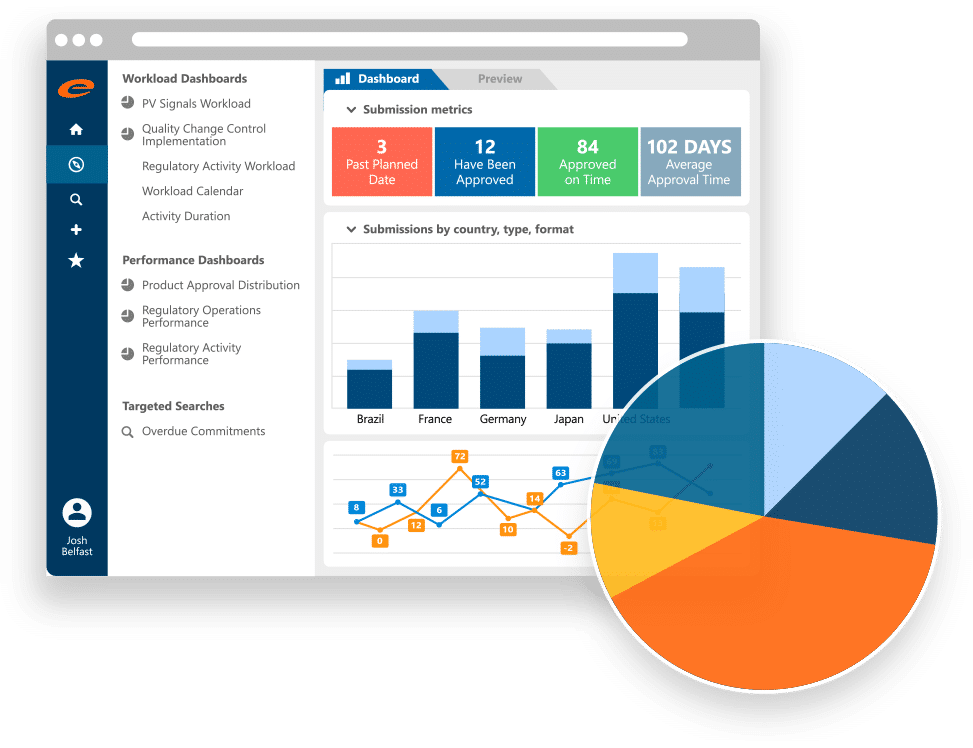
Ennov RIM — 全球法规信息管理仪表板,涵盖送件指针、国家分布与审核时程分析
应用领域
制药
eCTD 送件建构、文件生命周期管理、法规出版、NDA/ANDA/BLA/MAA 申请。
生物科技
IND/BLA 送件、法规文件组装、多区域送件管理。
学名药
ANDA 送件、经济实惠的 eCTD 出版方案。
委托研究机构(CRO)
为委托者提供出版服务、多客户送件管理。
动物保健
兽医 NeeS(VNeeS)送件、法规合规。
医疗器材
eCopy 送件(510(k)、PMA)。
竞争比较
| 功能 | Ennov | Lorenz docuBridge | Certara GlobalSubmit | Veeva Vault Submissions |
|---|---|---|---|---|
| 部署方式 | 云端、本地、混合 | 本地或托管 | 仅云端 SaaS | 仅云端 SaaS |
| eCTD 4.0 | 11 次试点(EMA/FDA/PMDA) | 前向兼容 | 已就绪 | 已就绪 |
| 集成 EDMS | 原生(Ennov Doc) | 外部 | 无 | 原生(Vault) |
| 验证器 | 内置(EMA 核准) | 捆绑(eValidator) | 内置 | 内置 |
| AI 功能 | 是(原生,v11.0) | 有限 | 有限 | 中等 |
| 送件传承 | 100 万+(Calyx/InSight) | 未揭露 | 150 万+ | 未揭露 |
关键差异化因素
三层产品组合
唯一提供自助式 SaaS(eCTD247)、企业原生(Dossier)和企业收购方案(InSight Publishing)的供应商 — 从新创到前五大药厂全覆盖
eCTD 4.0 领先地位
仅 4 家完成 EMA 试点的供应商之一;11 次试点送件为业界最高之列
快速创造价值
eCTD247 Premium「数天内」即可上线运作,含 30 天免费试用。云端模式宣称可降低 48% 成本
100 万+ 送件传承
Calyx/InSight Publishing 超过 100 万次全球法规送件的纪录,部署灵活性支持云端或本地随时切换

eCTD247 电子签章 — 符合 21 CFR Part 11 的文档签署、分发与生命周期管理
客户与产业验证
| 指针 | 数据 |
|---|---|
| 生命科学客户 | 450+ 家 |
| 全球用户 | 500,000+ |
| 全球法规送件 | 100 万+ 次(通过 Calyx/InSight 传承) |
| 项目准时交付率 | 98.5% |
| 维护续约率 | 96% |
| 客户稽核成功率 | 100% |
相关产品推荐
了解 eCTD247
加速您的药品上市申请流程,确保全球法规合规,立即体验 30 天免费试用
联系我们了解更多